![mosaics[1]](https://popsci.com.tr/wp-content/uploads/2025/02/mosaics1-696x392.jpg)
Vücudunuzu gözünüzün önüne getirin: Vücudunuz ömür boyunca biriken binlerce genetik hata taşıyan bir hücre koleksiyonudur. Bu hataların pek çoğu zararsız, bazıları zararlıdır ve en az birkaçı da sizin için iyi olabilir.
Bu makale aslen Knowable Magazine‘de yer alıyor.
Yumurta ve sperm birbiriyle buluştuğunda ve biyolojik ebeveynlerinizin DNA’sı beraber bir takım oluşturduğunda başladınız. İlk hücreniz yeni harmanlanmış genomunu kopyalamaya ve bölünerek bir vücut inşa etmeye başladı.
Ayrıca neredeyse hemen genetik hatalar birikmeye başladı.
İngiltere Hinxton’daki Wellcome Sanger Enstitüsünde kanser biyoloğu olarak çalışan Phil H. Jones, “Bu hataların genomunuzda birikme süreci yaşam boyu devam eder” diyor.
Bilim insanları DNA kopyalama sistemlerinin ara sıra hata yaptığını uzun süredir bilse de (kanserler sık sık böyle başlıyor); teknoloji sadece kısa süre önce her genetik yanlışın sınıflandırılacağı kadar hassas hale geldi. Üstelik hatalarla dolu olduğumuz ortaya çıktı. Her insan, bir hücre veya hücre grubundan diğerine kadar çoğunlukla birbirinin aynısı olup tek tük farklılıklar gösteren devasa bir hücre mozaiği.
Hücresel genomlar bir noktada tek bir genetik harf ile ve başka bir noktada ise kayıp olan daha büyük bir kromozom parçasıyla farklılık gösterebilir. Worcester’daki Massachusetts Chan Tıp Fakültesinde çalışan moleküler biyolog Michael Lodato, orta yaş itibarıyla vücudun her hücresinin muhtemelen bin kadar genetik yazım hatası barındırdığını tahmin ediyor.
Bu mutasyonlar (ister kanda olsun, ister ciltte veya beyinde), hücrenin DNA kopyalama mekanizması olağanüstü derecede isabetli olsa ve hücreler mükemmel onarım mekanizmaları sergilese bile ortaya çıkıyor. Yetiştkin bir vücut, 4 milyonu her saniye bölünen yaklaşık 30 trilyon hücre içerdiğinden, nadir hatalar bile zamanla birikiyor. (Hatalar, yumurta ve spermleri ortaya çıkaran hücrelerde çok daha seyrek; görünüşe göre vücut, mutasyonları üreme dokularından uzak tutmak için daha çok çaba ve enerji harcıyor ki gelecekteki nesillere bozulmamış DNA aktarılsın.)
“Hepimizin bu kadar iyi devam ediyor olması küçük bir mucize” diyor Jones.
Bilim insanları bu mutasyonların sebep ve sonuçlarını araştırmanın hâlâ erken aşamalarında. ABD Ulusal Sağlık Enstitüleri, bunların kataloglanması için 140 milyon dolar sermaye ayırmış. ABD Ulusal Zihin Sağlığı Enstitüsü ise beyindeki mutasyonların incelenmesine on milyonlarca dolar harcıyor. Pek çok değişim muhtemelen zararsız olsa da bazıları, kanserler ve nörolojik hastalıklar bakımından sonuçlar doğurabilir. Daha temelinde ise bazı araştırmacılar, yaşlanma sürecinin büyük bir kısmının altında ömür boyu gerçekleşen rastgele genomik hataların olabileceğinden şüpheleniyor.
“Bunu bileli on yıl bile olmuyor ve yeni bir kıtanın keşfedilmesine benziyor” diyor Jones. “Bütün bunların ne anlama geldiği konusunda henüz yüzeysel şeyler biliyoruz.”
Baştan şüpheli
Bilim insanları üreme dışı veya somatik dokularda biriken genetik yazım hataları ve diğer mutasyonların, hastalıkları ve yaşlanmayı açıklamaya yardımcı olabileceğinden DNA’nın yapısının keşfedildiği 1950’lerden bu yana şüpheleniyor.
1970’lerde araştırmacılar, hücrelerin bir bölümünde büyümeyi teşvik eden mutasyonların kanserlerin kökeni olduğunu biliyordu.
New York’taki Albert Einstein Tıp Fakültesinde çalışan genetikçi Jan Vijg, “Bu olayın frekansının çok ama çok düşük olduğu varsayılıyordu” diyor.
Fakat bu mutasyonları tespit edip incelemek son derece zordu. Standart DNA dizilemesinde, sadece geniş hücre gruplarından çıkarılan büyük miktarlardaki genetik malzeme analiz edilebiliyor ve sadece en yaygın dizilimler ortaya çıkarılıyordu. Nadir mutasyonlar ise radara girmiyordu. Kaliforniya’daki Stanford Üniversitesinde çalışan kök hücre biyoloğu Siddharta Jaisval, bu durumun 2008 civarında değişmeye başladığını söylüyor. Yeni teknikler o kadar hassas ki, hücrelerin ufak bir kısmında (hatta tek bir hücrede) bulunan mutasyonlar bile ortaya çıkarılabiliyor.
Jaisval 2010’ların başlarında, mutasyonların kan kanserine dönüşmeden önce insanların kan hücrelerinde nasıl birikebildiğiyle ilgileniyormuşb. 17.000’den fazla kişinin kanını inceleyen Jaisval ve meslektaşları, tahmin ettikleri şeyi bulmuş: Kanserle ilişkili mutasyonlar 40 yaşın altındakilerde nadirken, yaş ile beraber daha yüksek miktarlarda görülüyor ve 70’nci yaş gününden sonra kan hücrelerinin yaklaşık yüzde 10’u veya daha fazlasını oluşturuyorlarmış.
Fakat araştırma takımı, genelde mutasyonlu hücrelerin genetik olarak birbirinin aynısı olduğunu da görmüş: Bunlar klonmuş. Jaisval bunun sebebinin, vücudun kan üreten binlerce kök hücresinden birinin, büyüme ve bölünmede kendini biraz daha iyi hale getiren mutasyonları seçmesi olduğunu düşünüyor. Bu hücre normal şekilde büyüyen kök hücrelere onlarca yıl içerisinde galip gelerek, genetik olarak uyumlu büyük bir hücre grubu meydana getiriyor.
Etkili biçimde bölünen bu mutasyonlu kan hücresi klonları, doğal olarak kan kanseri tehlikesiyle ilişkilendirilmiş. Fakat aynı zamanda kalp hastalığı, inme ve herhangi bir sebepli ölümde risk artışıyla da (belki de enflamasyonu teşvik ettikleri için) ilişkilendirilmişler. Ayrıca beklenmedik bir şekilde, Alzheimer demansı riskinin üçte bir kadar azalmasıyla ilişkilendirilmişler. Kan hücresi klonlarının sağlığa etkileri üzerine 2023 Annual Review of Medicine bülteninde yayımlanan bir makalenin eş yazarlığını yapan Jaisval, bazı klonların beyin dokusunda çoğalma veya toksik proteinleri temizleme konusunda daha iyi olabileceğini düşünüyor.
Jaisval ve meslektaşları 2014 yılında rapor ettikleri bu kan klonlarını takip ederken, Wellcome Sanger Enstitüsünde çalışan araştırmacılar da göz kapağı derisiyle başlayarak diğer dokulardaki vücut mutasyonlarını incelemeye başlamışlar. Bazı insanların göz kapakları yaş ile birlikte sarkıyor ve bu sorunun düzeltilmesi için bir miktar cilt ameliyatla alınıyor. Araştırmacılar dört bireyden bu parçaları alarak, genetik dizileme için 1 ya da 2 milimetrelik daireler kesmiş. Wellcome Sanger’da çalışan genetikçi Inigo Martincorena, “Sürprizlerle doluydu” diyor. Hastalarda cilt kanseri olmasa da ciltleri binlerce klonla doluymuş ve göz kapağı cilt hücrelerinin beşte birinden üçte birine kadarı, kanserle ilişkili mutasyonlar barındırıyormuş.
Cilt kanseri olmayan insanlardaki bu kadar fazla cilt kanserinde mutasyon olduğunu gösteren bulgular büyük ilgi çekmiş. Colorado Üniversitesi Tıp Fakültesinde kanser biyoloğu olarak çalışan ve söz konusu çalışmada yer almayan James DeGregori, “Ağzım acık kalmıştı” diyor.
Wellcome Sanger araştırmacıları ise yemek borusu, mesane ve kalın bağırsağın da içinde bulunduğu diğer çeşitli dokularda birbirinin aynısı olan, mutasyon geçirmiş hücreleri belirlemeye başlamışlardı. Örneğin, bağırsak duvarındaki girintiler olan kolonik girintileri incelemişlerdi. Bunlardan her insanda yaklaşık 10 milyon tane var ve her biri yaklaşık 2.000 hücre barındırıyor. Bu hücrelerin de her biri, o girintide yer alan bir avuç kök hücresinden ortaya çıkıyor. 42 kişide 2.000’den fazla girintinin incelendiği bir çalışmada araştırmacılar, 50’li yaşlarda olan insanların girinti yapılarında yüzlerce genetik varyasyon bulmuş.
Bu yaş grubunda diğer türlü normal olan girintili yapıların yüzde 1 kadarı, kanserle bağlantılı mutasyonlar içeriyormuş. Söz konusu mutasyonların bazıları, civardaki hücrelerin yayılmasını baskılayarak mutant hücrelerin girinti yapısını daha çabuk ele geçirmesine imkan tanıyor. Bu durum tek başına kalın bağırsak kanseri oluşturmak için yeterli olmayabilir ama nadir vakalarda hücreler, kansere sebep olan ek mutasyonlar kazanarak girinti yapısının sınırlarından taşıp kötü huylu tümörlere sebep oluyor.
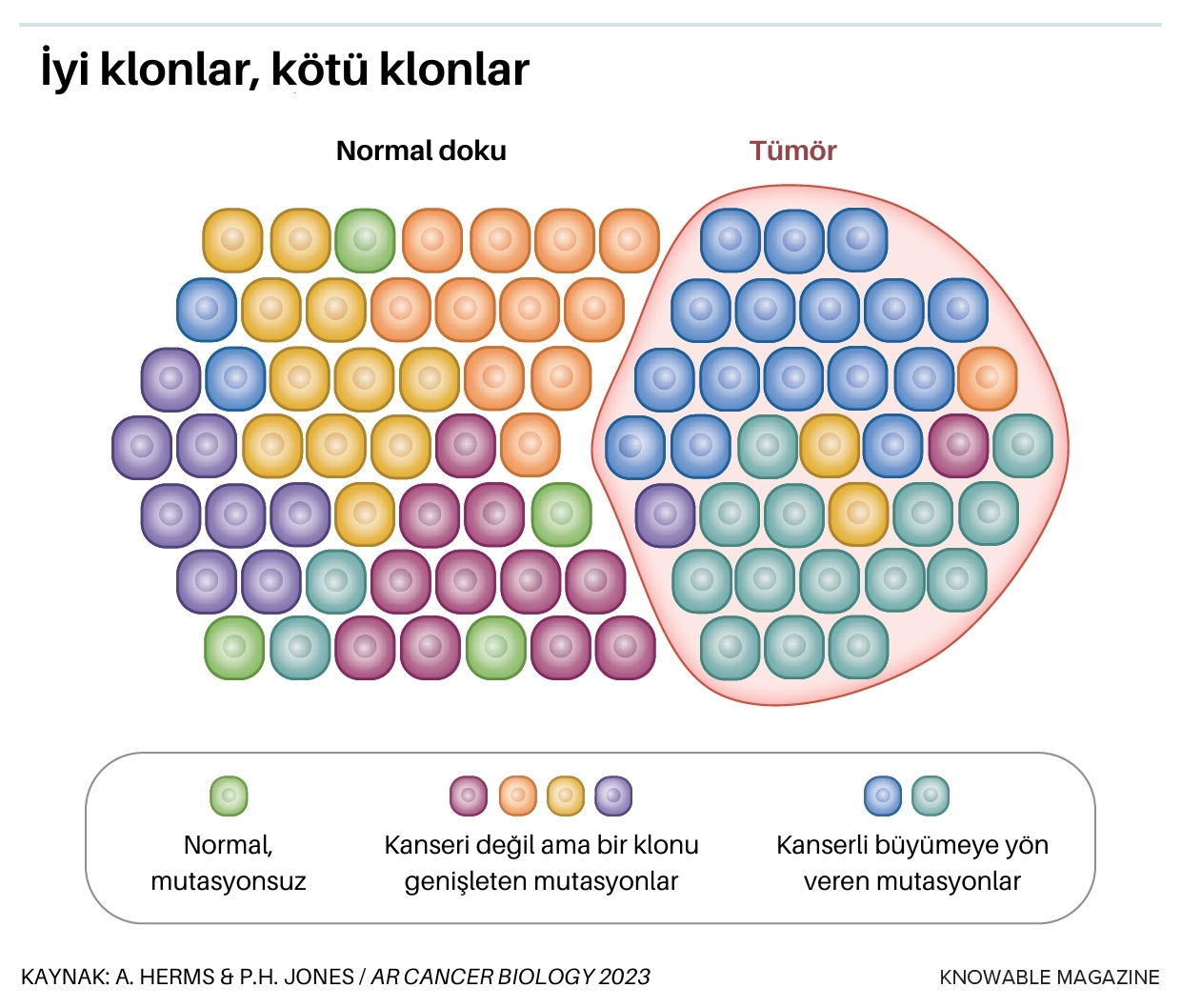
“İnsanlar bu somatik mutasyonları her yerde aradı ve onları her organda bulduk” diyen Jones, vücudu bir çeşit evrimsel savaş meydanı gibi görüyor. Hücreler mutasyon biriktirdikçe, daha fazla (veya daha seyrek) büyüyüp bölünebiliyorlar. Daha kolay çoğalan bazı hücreler, zamanla diğerlerini geride bırakabiliyor ve geniş klonlar oluşturabiliyor.
“Ayrıca” diye belirtiyor DeGregori, “yumrulu bir şeye dönüşmüyoruz.” Dokularımızın, klonların kansere dönüşmesini engelleyen yöntemleri olması gerektiğini ileri sürüyor. Aslında Jones ve diğer makale yazarının 2023 Annual Review of Cancer Biology bülteninde tarif ettikleri üzere, farelerde fazla büyüyen mutant klonların normal büyümeye geri döndüğü görülmüş.
Jones ve meslektaşları, insanlardaki yemek borusunda bir koruma örneği keşfetmişler. Genelde yemek borusu dokusunun büyük bir kısmını oluşturan pek çok klon, orta yaş itibarıyla NOTCH1 adı verilen bir geni bozan mutasyonlara sahip. Bu durum yemek borusunun yiyecekleri taşıma kabiliyetini etkilemiyor ama kanserlerin büyümek için NOTCH1‘e ihtiyacı olduğu görünüyor. Yemek borusu hücrelerinde kötü mutasyonlar birikebiliyor fakat NOTCH1 olmadığında, tümöre dönüşme ihtimalleri daha düşük gibi duruyor.
Diğer bir ifadeyle bedensel mutasyonların bazıları kötü veya nötr değil, hatta faydalı. Ayrıca neyse ki bu iyi mutasyonlar çoğu zaman galip geliyor.
Beynin içerisine girmek
DNA koplama mekanizmamızın yemek borusu, kalın bağırsak ve kan hücrelerinde hata yapma bakımından pek çok olanağı var çünkü bunlar sürekli bölünüyor. Fakat beynimizdeki nöronlar, doğumdan önce veya kısa süre sonra bölünmeyi bırakıyor. Boston Çocuk Hastanesinde nörogenetikçi olarak çalışan Christopher Walsh, bu yüzden bilim insanlarının esasında bunların genetik açıdan bozulmamış kaldıklarını varsaydıklarını söylüyor.
Fakat yaşam boyunca biriken mutasyonların beyinde problemlere sebep olabileceğini gösteren işaretler var. Araştırmacılar 2004 yılında, sadece bazı beyin hücrelerinde bulunan bir mutasyon sebebiyle Alzheimer hastalığı olan bir hasta rapor etmiş. Bu mutasyon yeniymiş ve her iki ebeveynden de geçmemiş.
Ayrıca 2012 yılında Walsh’ın grubu, beyinde fazla büyüyen ve nöbetlere sebep olan bir yeri düzeltmek için yaptıkları ameliyat sırasında alınan beyin dokusu üzerinde bir analiz yürütmüş. Sekiz numuneden üçünde, beyin boyutunu düzenleyen bir geni etkileyen mutasyonlar varmış ancak bu mutasyonların kanda devamlı bulunmaması, vücudun sadece bir kısmında ortaya çıktıklarını akla getiriyor.
Lodato, beyin hücrelerinin çeşitli şekillerde mutasyon kazanabileceğini söylüyor. Bir mutasyon gelişimin erken aşamasında, beyin tamamlanmadan ve hücreleri bölünmeyi durdurmadan önce ortaya çıkabilir. Ya da erişkin bir beyin hücresinde DNA hasar görebilir ve düzgün onarılmayabilir.
2012 yılında kalıtımla geçmeyen beyin mutasyonlarına olan ilgi artmaya başlamış. O zamanlar ABD Ulusal Zihin Sağlığı Enstitüsü başkanı olan Thomas Insel, pek çok psikiyatrik durumun altında bu tür mutasyonların yatıyor olabileceğini öne sürmüş. Beyindeki bu katılımla alınmamış mutasyonlar, nörolojik hastalıklarda uzun süredir var devam eden bir bilmeceyi açıklığa kavuşturabilir: Mesela neden tek yumurta ikizlerine genelde aynı psikiyatrik teşhisler konmuyor? (örneğin ikizlerden birinde şizofreni gelişirse, diğerinde hastalığın ortaya çıkma ihtimali sadece yüzde 50 kadar).
San Diego’da bulunan ve epilepsinin şiddetli bir türüyle ilgili yapılan araştırmaları ve aileleri destekleyen, kâr amacı gütmeyen Lennox-Gastaut Sendromu Vakfı’nın bilimsel direktörü sinirbilimci Mike McConnell, mozaikliğin “çok ikna edici bir cevap sunduğunu” söylüyor.
McConnell, Walsh, Lodato ve diğerleri, 2010’ların başlarından itibaren hayatını kaybeden insanların beyinlerine serpilmiş büyüklü küçüklü mutasyonları sınıflandırmaya başlamışlar. Genlerin, birden fazla genin veya kromozomların tamamının delesyon ve kopyalarının tek tek çetelesini tutmuş; genomda yeni noktalara giden kromozom bölümlerini bütünüyle belirlemişler. Walsh, Lodato ve meslektaşları nihayetinde, 50’li yaşlardaki kişilerin her bir sinir hücresinin genetik kodunda bin veya daha fazla tek harifli mutasyon olduğunu keşfetmiş. O son bulgunun “Tamamen imkansız göründüğünü” anımsıyor Walsh. “Kendimizden şüphe duymuştuk.”
Böylesine çarpıcı sonuçların karşısında bilim insanları daha da fazlasını araştırmış. Yaşları dört aylık ile 82 arasında değişen ve vefat etmiş 15 kişiden alınan 159 nörona bakmışlar. Araştırmacılar mutasyon sayılarının yaşla beraber arttığını ve bu durumun da hataların, vücudun diğer kısımlarında olduğu gibi zamanla arttığını gösterdiğini bildiriyor. “Beyin, büyük ve derin biçimde bir mozaik” diyor Lodato.
ABD Ulusal Zihin Sağlığı Enstitüsü, bu mozaikliği daha da fazla araştırmak için 2015’ten 2019’a kadar yürütülen bir dizi projeye fon sağlamış. Bu projelerde, genellikle ölümden sonra toplanan ve doku bankalarına yatırılan, nörotipik veya Tourette sendromu ve otizm tayf bozukluğu gibi durumlara sahip 1.000’i aşkın kişiye ait numunelerde beyin dokusunun mozaikliği araştırılmış.
Projenin eş öncülüğünü yürüten McConnell, tek harfli mutasyonların en yaygın olduğunu söylüyor. Araştırmacılar 400 terabaytı aşkın DNA dizilim verisi ve başka veriler toplayıp analitik araçlar geliştirerek, beyin mozaikliği çalışmalarında bir sonraki turun inşa edileceği güçlü bir platform oluşturmuş. Bilim insanları bu ve diğer çalışmalardan, beyin mozaikliği ile otizm, epilepsi ve şizofreni gibi nörolojik hastalıkları ilişkilendirmiş.
Lodato’nun laboratuvarında çalışan yüksek lisans öğrencileri Cesar Bautista Sotelo ve Sushmita Nayak, biriken mutasyonların felç edici bir durum olan amiyotrofik lateral skleroza nasıl sebep olabileceğini araştırıyor. Genetikçiler, kalıtımsal olmayan vakaların sadece yüzde 10 kadarında bilinen bir mutasyon belirleyebiliyor. Fakat mozaikliğe yönelik yeni veriler, daha pek çok insanın beyinleri veya omuriliklerindeki ALS genlerinde mutasyonlar olabileceğini akla getiriyor; bunlar vücutlarının geri kalanında olmasa bile.
Bu önemli çünkü bilim insanları, mutasyon geçirdikleri zaman ALS’ye sebep olan 40’ı aşkın genin bazılarının hedef alındığı terapiler üzerinde çalışıyor. Gıda ve İlaç Dairesi, mutasyon geçiren yaygın bir ALS genini kapatan böyle bir tedaviyi 2023 yılında ilk defa onaylamıştı. Hastaların bu gibi terapilere hak kazanması için mutasyonlarını bilmeleri gerekecek.
Bu yüzden, diyor Nayak, “ALS teşhisindeki mevcut uygulamanın değiştirilmesini güçlü biçimde savunuyoruz.” Sadece bir kan numunesindeki DNA’ya bakmak yerine, kanı değil de vücuttaki dokuları meydana getiren hücrelerin gelişimi esnasında bir ALS mutasyonu ortaya çıkarsa diye tükürük, saç veya cilt gibi diğer dokular da incelenebilir.
Nasıl yaşlandığımıza dair ipuçları
Şimdilik, vücudumuzdaki mozaikliğin sağlık açısından doğurduğu sonuçlar çoğunlukla eylem gerektirecek kadar net değil; özellikle de sunulacak alakalı bir tedavinin olmadığı kan klonları gibi durumlarda. “İnsanların bu konuda endişelenmesi gerektiğini savunmuyoruz aslında” diyor Jaiswal. “Zamanın bu noktasında, sağlıklı olan insanları test etmenin bir mantığı yok.”
Fakat pek çok bilim insanına göre bulgular, uzun süredir var olan bir kuramın kanıtı niteliğinde: Bir yaşam boyu oluşan mutasyonlar, yaşlanma şeklinde adlandırdığımız kaçınılmaz şeye yol açıyor.
Martincorena ve meslektaşları, 2022 tarihli bir çalışmada bu kuramın öğelerinden birini test etmiş. Eğer mutasyon birikimi yaşlanmaya katkıda bulunuyorsa, o halde fare gibi kısa ömürlü mutasyonlar hızlı birikirken insanlar gibi daha uzun ömürlü türlerde, belki de onarım mekanizmalarının daha iyi olması sebebiyle mutasyonların daha yavaş biriktiğini öne sürmüşler.
Araştırmacılar bu fikri araştırmak üzere, sekiz insan ve ayrıca bir canlı koleksiyonundan alınan kalın bağırsak girinti numunelerini inceledikleri beş yıllık bir yolculuğa çıkmışlar. Söz konusu canlılar arasında 19 laboratuvar faresi ve sıçan; kediler, köpekler, inekler ve tavşanlar gibi 15 evcil hayvan; kaplanlar, lemurlar, bir liman yunusu ve 30 yıldan fazla yaşamasıyla bilinen tüysüz köstebek farelerinin yer aldığı 14 egzotik hayvan daha var. Tahmin edildiği gibi tür ne kadar uzun yaşıyorsa, mutasyonların birikimi de o kadar yavaş oluyor.
Araştırmacılar birkaç türe ait kalın bağırsak girintisini analiz ederek, daha uzun yaşayan türlerde mutasyonların daha yavaş biriktiğini belirlemiş. Bu durum, yaşlanmayla ilişkilendirilen vücut hücresi mutasyonlarına dair uzun süredir var olan bir kuram ile tutarlılık gösteriyor.
“Bu durum somatik mutasyonların yaşlanmaya sebep olduğunu göstermiyor fakat en azından bir miktar rol oynadıkları ihtimaliyle tutarlılık sergiliyor” diyor Martincorena. Bu noktada iş başında olan iki unsur var: Mutasyonların birikmesi ömrün daha kısa olmasına katkıda bulunuyor fakat sonrasında bu kısalan ömür, mutasyon korumasının önemini azaltıyor; dolayısıyla kısa ömürlü türlerde, DNA onarımına daha düşük yatırım oluyor.
Mutasyonların yaşlanmaya katkıda bulunabileceği fikri, onları mağlup etmenin genetik bir gençlik çeşmesi olabileceğini akla getiriyor. “Eğer yarın öbür gün bu mutasyonların birikmesini durdurmanın bir yolunu bulursam, inanılmaz zengin olurum” diyor Bautista Sotelo. Halihazırda en az bir biyoteknoloji startup’ı (New York’taki Matter Bio), insan genomunu onarma hedefiyle fon toplamış. (Böyle bir planın o kadar geniş bir hücre yığınında uygulanıp uygulanamayacağı başka bir mesele: “Mutasyonlardan kurtulabileceğinizi sanmıyorum” diyor DeGregori.)
Vücuttaki mutasyonların hikayesi sona ermekten çok uzakta. “Şu an yaptığımız keşiflere bakarsak, yolculuk daha yeni başladı” diyor Martincorena. “Önümüzdeki birkaç yıl içinde pek çok sürpriz bekliyorum.”
Yazar: Amber Dance/Knowable Magazine. Çeviren: Ozan Zaloğlu.




