Bir kimyacı, periyodik tablonun 150’nci yıl dönümünde geriye bakıp çeşitli tabloları inceliyor.
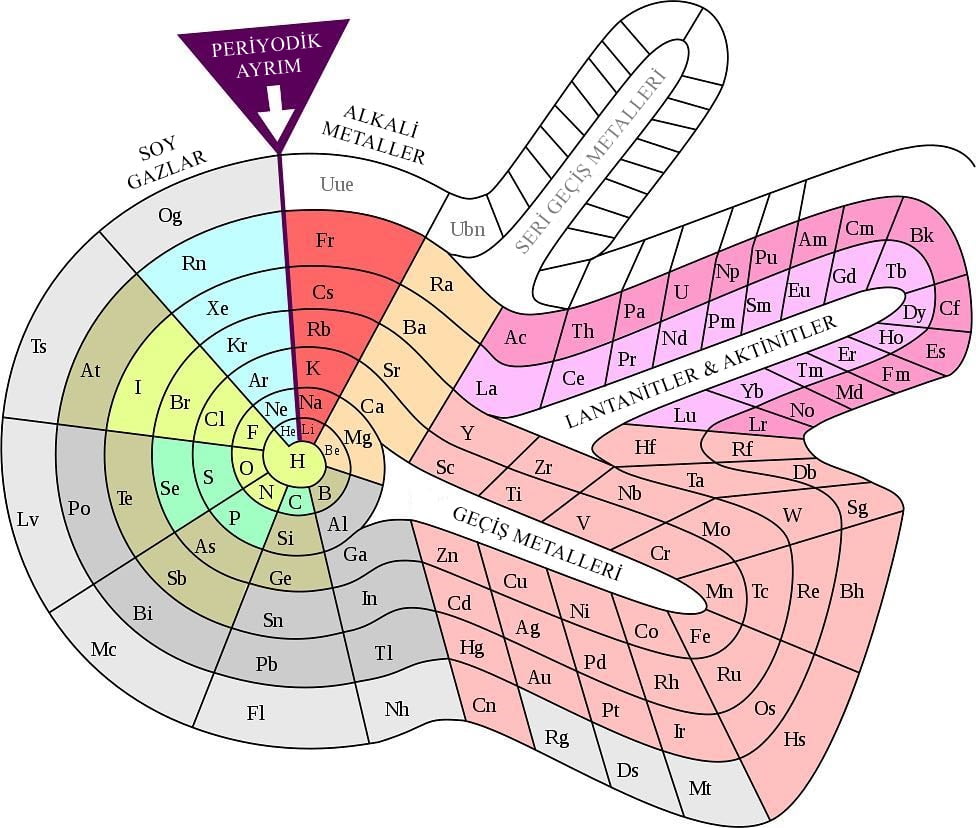
Periyodik tablo, neredeyse her kimya laboratuvarının duvarlarından öğrencilere bakıyor. Tabloyu oluşturan kişinin, genelde Dimitri Mendeleev olduğu düşünülür.

Rus kimyacı, (o zamanlar sadece 63 tane olan) bilinen elementleri kartlara yazmış ve onları, kimyasal ve fiziksel niteliklerine göre sütun ve sıralara koymuştu. BM, bilimdeki bu çok önemli noktanın 150’nci yıldönümünü kutlamak amacıyla, 2019 yılını Uluslararası Periyodik Tablo yılı ilan etti.
Fakat aslında, periyodik tablo Mendeleev ile başlamamıştı. Pek çok kişi, elementleri kurcalayıp onları sıralamakla uğraşmıştı. Kimyacı John Dalton, onlarca yıl önce bir tablo oluşturmayı denemiş ve ayrıca elementler için bazı ilginç simgeler yapmaya çalışmıştı (fakat bunlar tutulmadı). Ayrıca Mendeleev, ev yapımı kart destesi işine koyulmadan sadece birkaç yıl önce; John Newlands da elementlerin özelliklerine göre sıralandığı bir tablo yapmıştı.
Mendeleev’in yeteneği, masada bıraktıklarında saklıydı. Belirli elementlerin kayıp olduğunu ve henüz keşfedilmediğini fark etti. Bu yüzden Dalton, Newland ve diğerleri; bilinen şeyleri hazırlarken, Mendeleev ise bilinmeyenler için boş yer bırakmıştı. Daha şaşırtıcı olanı ise, kayıp elementlerin özelliklerini doğru şekilde tahmin etmesiydi.

Mendeleev’in yukarıdaki tablosunda yer alan soru işaretlerini fark ettiniz mi? Örneğin, Al (alüminyum) elementinin yanında, bilinmeyen bir metal için yer bırakılmış. Mendeleev, bunun atomik kütlesinin 68 olacağını, bir santimetre küpte altı gram yoğunlukta olacağını ve çok düşük bir erime noktasının bulunacağını tahmin etmiş. Paul Émile Lecoq de Boisbaudran, altı yıl sonra galyum elementini ayırmış ve element gerçekten tam da bu boşluğa oturmuş; 69.7’lik bir atomik kütlesi, 5.9 g/cm³’lük bir yoğunluğu ve elinizde sıvı hale gelecek kadar düşük bir erime noktası varmış. Mendeleev, aynı şeyi skandiyum, germanyum ve teknetyum için de yapmış (teknetyum, kendisi öldükten 30 yıl sonra, 1937’de keşfedilmiş).
Mendeleev’in tablosu, ilk bakışta bizim aşina olduğumuz tabloya pek benzemiyor. Bir kere; çağdaş tablo, Mendeleev’in gözden kaçırmış olduğu (ve yer bırakmadığı) bir sürü element içeriyor. Bunlardan en göze çarpanı, soy gazlar (helyum, neon ve argon gibi). Ayrıca tablo, çağdaş şekline göre farklı yöne gidiyor: Artık sütunlara koyduğumuz elementler, orada sıralara konmuş.
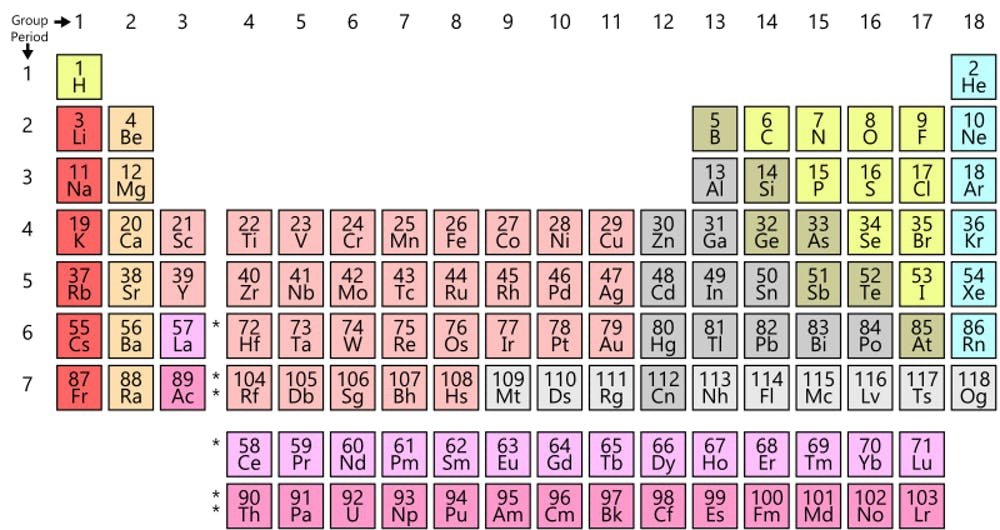
Fakat Mendeleev’in tablosunu 90 derece döndürdüğünüz zaman, çağdaş şekille olan benzerlikler belli oluyor. Örneğin halojenlerin (flor [F], klor [Cl], brom [Br] ve iyot [I] [Mendeleev’in tablosunda J simgesi]) hepsi, birbirlerinin yanında görünüyor. Bugün ise tablonun 17’nci sütununda dizilmişler (veya kimyacıların söylemeyi tercih ettiği üzere, 17. grupta).
Deneme Periyodu
Bu tablodan, bilindik şemaya yapılan geçiş, küçük bir sıçrama gibi görünebilir fakat Mendeleev’in yayınlarından yıllar sonra, başka element düzenleriyle çok sayıda deneme yapılmıştı. Tablo, dik açılı ve kalıcı şeklini almadan önce; ahali bazı ilginç ve muhteşem çözümler teklif etmişti.

Özellikle dikkat çekici olan bir örnek ise; Heinrich Baumhauer’ın 1870’de yayınlanan, merkezinde hidrojenin yer aldığı ve atom kütleleri giderek artan elementlerin dışa doğru sarmal şeklinde uzandığı sarmal tablosuydu. Tekerin her bir parmaklığına düşen elementler, günümüzün tablosunda olduğu gibi; bir sütunda (grup) bulunanlar ile ortak özellikleri paylaşıyordu. Henry Basset’in 1892 yılında yaptığı ve epey ilginç olan “gülle” formülleştirmesi de vardı.
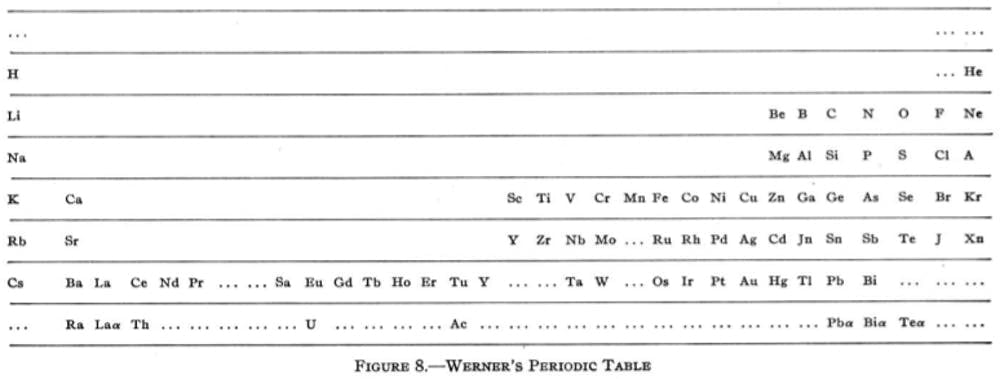
Bununla beraber tablo, 20’nci yüzyılın başında; Heinrich Werner’ın 1905 yılında yaptığı ve şaşırtıcı şekilde çağdaş görünen, tanıdık ve yatay bir biçime oturmuştu. Soy gazlar ilk defa, tablonun en sağında, şimdi aşina olduğumuz konumlarında görülmüştü. Werner ayrıca, boşluklar bırakarak Mendeleev’in kitabından bir yaprağı çıkarmayı da denemişti ancak aksine; hidrojenden ve hidrojen ile helyum arasında duran başka bir elementten daha hafif elementler önererek (ki hiçbiri mevcut değildi), tahmin yapma işini fazla kaçırmıştı.
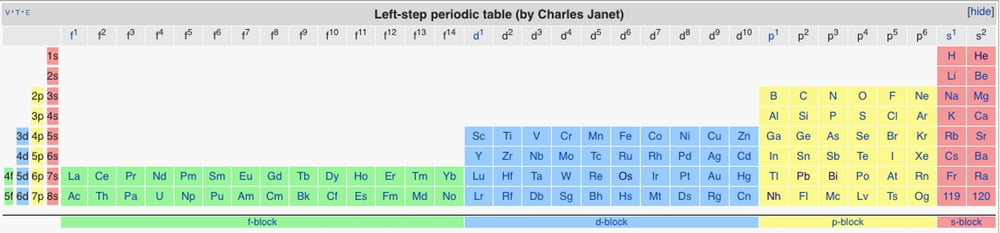
Bu tablonun epey çağdaş görünmesine rağmen, hâlâ bir miktar düzenlemenin yapılması gerekiyordu. Charles Janet’in yaptığı tablo, özellikle etkili olmuştu. Kendisi, bir fizikçinin bu tabloya karşı yaklaşımını almış ve yeni keşfedilen kuantum kuramını kullanarak, elektron gruplaşmalarına dayanan bir düzen oluşturmuştu. Bunun sonucunda ortaya çıkan “sol adımlı” periyodik tabloyu, hâlâ pek çok fizikçi tercih ediyor. İlginç şekilde Janet, o zamanlar sadece 92 element bilinmesine rağmen, 120 taneye kadar alan bırakmıştı (şimdilik yalnızca 118 tane var).
Bir tasarıma karar vermek
Çağdaş tablo, aslında Janet’in yaptığı tablonun doğrudan evrim geçirmiş bir şekli. Alkali metaller (en üstte lityumun bulunduğu grup) ve toprak alkali metaller (en üstte berilyumun yer aldığı grup), çok geniş görünen (uzun biçimli) bir periyodik tablonun oluşturulması amacıyla en sağdan en sola kaydırıldı. Fakat bu biçim, bir sayfa veya bir postere güzel sığmıyordu. Bu yüzden, çoğunlukla estetik sebeplerle; f blok elementleri genelde çıkarıldı ve ana tablonun altına yerleştirildi. İşte, bugün tanıdığımız o tabloya böyle ulaştık.
Fakat bu durum, ahalinin tablo düzenlerini kurcalamadığı anlamına gelmiyor; bunu da genelde, geleneksel tabloda kolayca göze çarpmayan elementlerin arasındaki ilişkileri vurgulamaya çalışarak yapmışlardı. Özellikle sarmallı ve 3 boyutlu olanların meşhur olduğu, yüzlerce çeşit bulunuyor (Mark Leach’in veritabanına bakın); esprili şekillerden bahsetmeyelim bile.

Peki benim, iki simgesel şekli; Mendeleev’in tablosu ile Henry Beck’in Londra Metrosu haritasını birleştirmeme ne demeli?
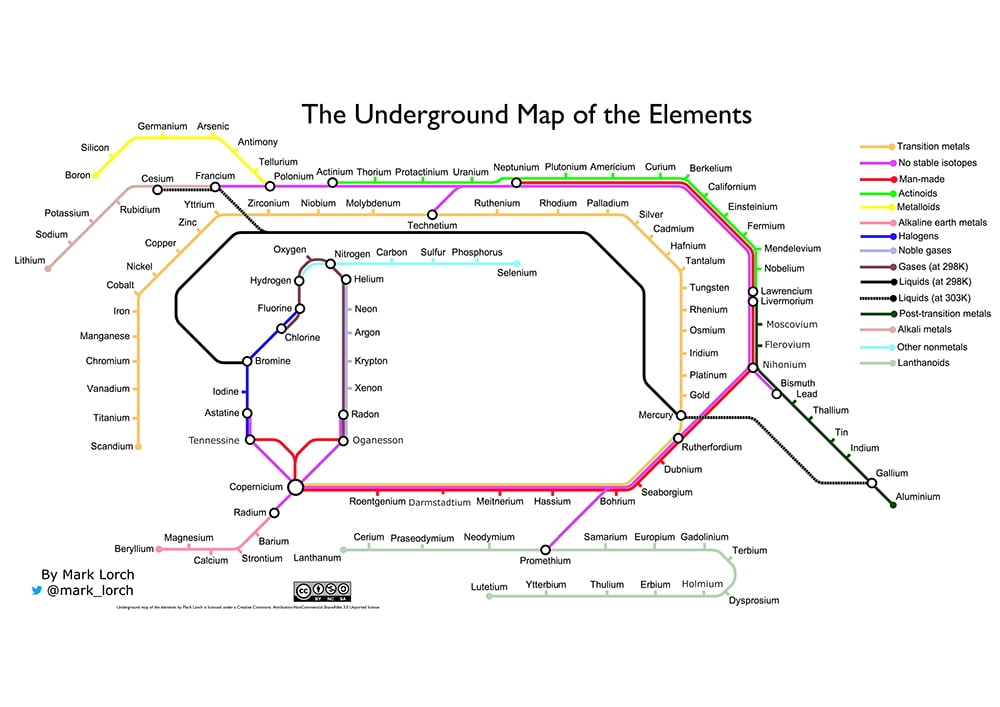
Ya da biradan Disney karakterlerine kadar her şeyi sınıflandırmaya karşı bilimsel bir his vermeyi hedefleyen, sersemletici taklit dizisi? Benim özellikle en sevdiğim; “mantıksız zırvalık“. Hepsi de; periyodik element tablosunun, bilimin nasıl meşhur bir simgesi haline geldiğini gözler önüne seriyor.
Mark Lorch, Hull Üniversitesi’nde Bilim İletişimi ve Kimya Profesörü.
The Conversation




