Nöro dejeneratif hastalıkta kritik bir molekül haritalandı.
Depositphotos
Bu ay Nature’da yayınlanan yeni bir çalışma, Alzheimer araştırmalarında kilometre taşı denebilecek kadar önemli yeni bir gelişmeyi duyurdu. Alzheimer hastalarının beyin hücrelerinde bulunan ve nöro dejeneratif hastalığın nedeni olarak düşünülen bir protein yapısının, tau iplikçiğinin, oluşturulan ilk komple modeli gösterildi.
Pek çok bilim insanı, tau proteinlerinin Alzheimer hastalığının moleküler yapı taşları olduğuna inanmaktadır. Hücrenin içinde bu proteinler birleşerek yığılır ve yumaklar oluştururlar. Bu yumakların hücre iletişimini engellediği, lezyonlar oluşturduğu ve nihayetinde Alzheimer ile ilişkili hafıza kaybına neden olduğu düşünülmektedir. Farklı tau proteini dizilimleri veya “morfolojileri”, Parkinson gibi farklı nöro dejeneratif hastalıklarla bir arada bulunmaktadır.
Cambridge’deki Tıbbi Araştırma Konseyi’nin Moleküler Biyoloji Laboratuvarı’ndan, bir grup araştırmacı yeni makale yayımlayarak, bu proteinlerin komple yapısını ilk defa haritaladılar. Araştırmacılar, tau iplikçiğinin aslında iki parçadan oluştuğunu keşfetti: Daha önce başka yöntemlerle tanımlanan katı bir çekirdek ve daha önce bilinmeyen hareketli parçaların “belirsiz kabuğu”. Makalede, proteinin C-şeklinde bükülmüş iki çiftli iplikten oluştuğu, aşağıdaki şema ile gösterilmektedir.
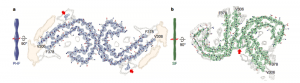
Tıbbi Araştırma Konseyi’nin Moleküler Biyoloji Laboratuvarı
Şimdiye kadar, tau kümelenmesini (semptom meydana getiren yumakların oluşumunda anahtar bir süreç) anlamak için sadece katı çekirdeğe bakmışlardı. Artık yapının tamamı çizildiğinden, araştırmacılar molekülün gerçekte nasıl çalıştığını daha iyi anlayabilecekler. Yapısal bir biyolog ve Cambridge ekibinin bir parçası olan Sjors Scheres, “Asıl katkı, esasen bu iplikçiklerin moleküler düzeyde, atom seviyesinde anlaşılması,” diyor.
Sonuçlar, Alzheimer araştırmacılarının, 34 yıldan fazladır sürdürdükleri çalışmalarının bir sonucudur. 80’li yıllardan beri tau proteinlerinin hastalığın önemli bir unsuru olduğunun farkında olmalarına rağmen, bilim insanları, mevcut yapıyı tam olarak haritalandıramadıklar- mevcut tekniklerle net bir görüntü elde edemediler. Cambridge ekibinin başarılı olmasını sağlayan ise, yeni icat, cryo elektron mikroskobu veya cryo-EM olarak adlandırılan bir süreçti (Scheres bu yöntemi burada ayrıntılı olarak açıklıyor). Mikroskoplar ve yazılımlardaki gelişmeler, bu atom-seviyeli görüntülerin çözünürlüğünü büyük ölçüde geliştirdi.
Aberdeen Üniversitesi’nde uzun zamandır Alzheimer araştırmaları yapan Claude Wischik “Bunu düşünmüştüm ve uzun süredir ilk prensiplerinden itibaren çözmeye çalışıyordum, ortaya çıkan bu çok güzel yapıyı hiç tahmin etmemiştim,” diyor. Şu anda bir ilaç tedavisi geliştirmek için çalışıyor, ancak bu yeni çalışmaya kendisi dahil değilmiş.
İlginçtir ki, C-şekilli yapının ucu, mantar prionları oluşturabilen ve Podospora anserina denilen bir maya türünün ucuna son derece benzemektedir- kendisi de kıvrık bir protein olup, bir şekilde kendi ayrıntılarını taklit etmesi için karşılaştığı sağlıklı proteinleri kandırabilmektedir. Yapı, her iki molekül türünün de bulaşıcılık özelliklerini gizler, potansiyel olarak tau proteinin, diğer sağlıklı proteinleri nöro dejeneratif hastalıkla ilişkendirilen, hastalıklı biçime dönüşmeye nasıl ikna edebildiğini açıkladığı anlamına gelebilir.
Wischik, “Prototip ilacımızın çalışacağı ve daha iyi ilaçlar bulabileceğimiz, molekülü tamamen keşfetme noktasına ulaşmamıza imkan tanıyabilir,” diye ekliyor. Küçük moleküllerin tau protein iplikçiğine girme ve hücrenin kurtulabileceği yapılara bölünmesini sağlama potansiyelleri konusunda özellikle umutluyuz.
Washington Üniversitesi, Tıp Fakültesi’nden araştırmacılar, Alzheimer ve uyku bozuklukları ile ilgili yeni çalışmalar yayımladıklarını (ilk duyurulduğu zaman üzerini kapamışlar) belirtti. Çalışmaları, tau iplikçiklerinin anlaşılmasının hastalığın sebebini bulmakta ne kadar önemli olduğu gerçeğini gözler önüne seren bir örnektir: Düzenli ve kesintili uykudan sonra beynin tau düzeylerini ölçüp, bir gece boyunca zararlı molekülleri temizleme yeteneğini araştırıyorlardı. Derin uykunun, tau kıvrımlarını zarar veremeyecek bir yerde tutmakta en önemli şey olduğu görüldü. Yüksek çözünürlükte tau yapısını görmek, derin uykuda temizlenmenin arkasındaki moleküler mekanizmaları anlamalarına yardımcı oldu.
Daha geniş bir açıdan bakmak gerekirse, etkili Alzheimer ilaçlarının hastalığa maruz kalanlara yardım etmesi uzun zaman alacaktır. Ancak cryo-EM sürecindeki ilerlemeler ve moleküler biyolog birçok bilim insanının özel çalışmaları ile harekete geçildiğinde, artık Alzheimer’in beyni nasıl etkilediğini tam olarak anlamak için bir başlangıç noktamız var. Bizim ve sevdiklerimizin, neden anıları ve bilişsel yetenekleri kaybettiğimizi anlamaya ve onu tedavi etmenin etkili bir yolunu bulmaya bir adım daha yaklaşıldı.